BE试验实行备案管理及BE预试验备案
在临床研究中,生物等效性(BE)试验是评估两种药物或治疗方法之间的相似性和等效性的关键步骤。为了确保BE试验的可靠性和准确性,许多国家和地区都制定了一系列规定和要求,其中包括BE试验实行备案管理及BE预试验备案。
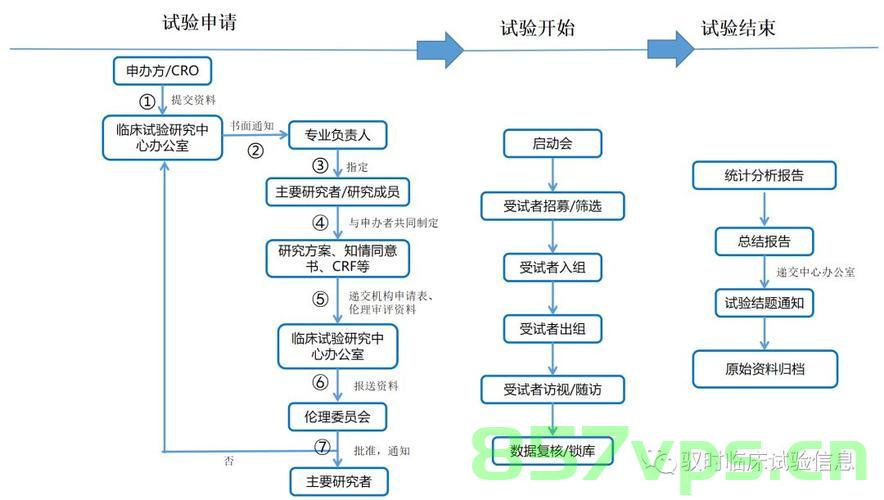
(图片来源网络,侵删)
BE试验实行备案管理是指在进行BE试验之前,研究者必须向相关机构提交相关文件并进行备案登记。这些文件包括研究计划、研究方案、研究人员资质、实验设备等信息。备案管理的目的是确保BE试验符合伦理规范和法律要求,保障受试者的权益和安全。
BE预试验备案是指在进行正式的BE试验之前,需要进行一系列的预试验来评估药物的安全性和有效性。这些预试验包括体外试验、动物实验和临床前研究等。通过BE预试验备案,可以有效地降低BE试验的风险和提高试验的成功率。

(图片来源网络,侵删)
在实施BE试验时,备案管理和预试验备案是非常重要的环节。通过严格的备案管理和预试验备案,可以确保BE试验的科学性、可靠性和可复制性,为新药的研发和临床应用提供可靠的依据。
BE试验实行备案管理及BE预试验备案是保障临床研究质量和安全性的重要措施,也是提高新药研发成功率的关键步骤。
文章版权声明:除非注明,否则均为VPS857原创文章,转载或复制请以超链接形式并注明出处。







还没有评论,来说两句吧...